Saúde
Inteligência artificilal antecipa diagnóstico de Alzheimer com precisão inédita
Modelo baseado em redes neurais de grafos alcança mais de 85% de acurácia e identifica padrões cerebrais antes dos sintomas clínicos mais graves
Imagem: Reprodução
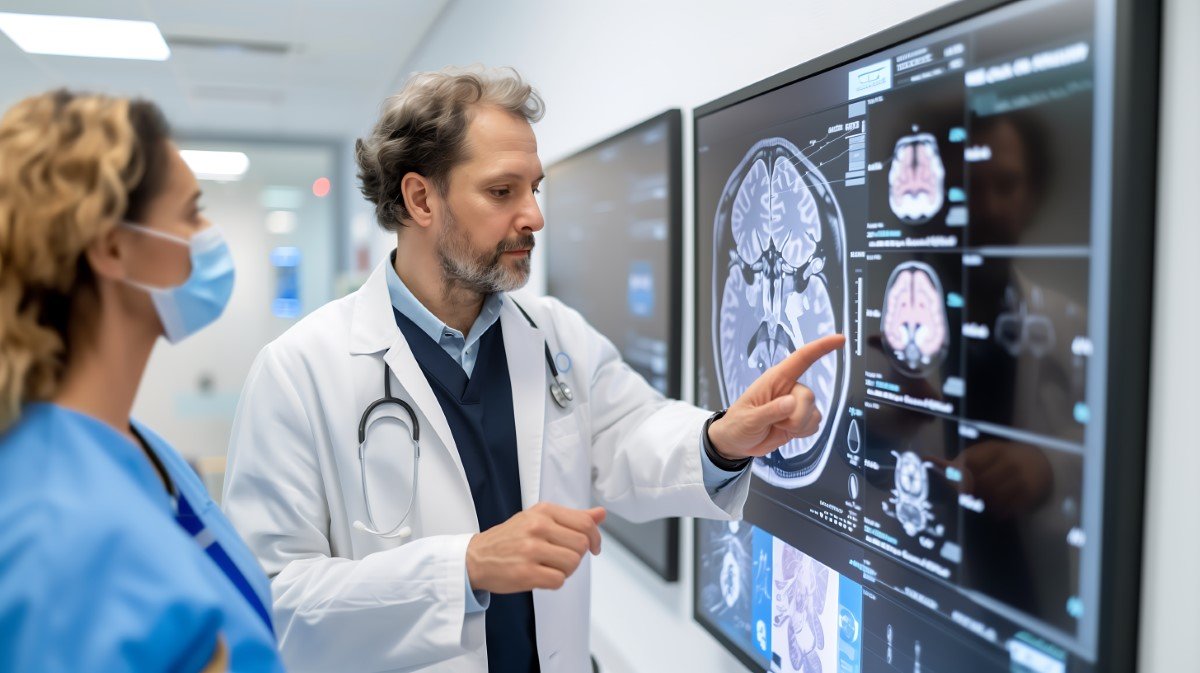
O diagnóstico precoce da doença de Alzheimer sempre esbarrou em um obstáculo central: detectar alterações cerebrais sutis antes que os sintomas cognitivos se tornem evidentes. Um novo estudo publicado neste sábado (25), na revista Scientific Reports, propõe agora uma virada nesse cenário ao apresentar um modelo de inteligência artificial capaz de identificar a doença em seus estágios iniciais com alto grau de precisão.
Desenvolvida por pesquisadores liderados pelo cientista Jinhua Sheng, da Universidade de Hangzhou Dianzi, na China, a tecnologia utiliza redes neurais de grafos — uma abordagem avançada de aprendizado de máquina — para analisar o cérebro como uma rede complexa de conexões. O método, batizado de ANA-GNN (Adaptive Neighborhood Aggregation Graph Neural Network), alcançou 85,23% de acurácia e 85,44% de F1-score na classificação de pacientes, superando modelos tradicionais e outras arquiteturas de ponta .
“O diagnóstico precoce do Alzheimer é crucial, mas extremamente desafiador devido às mudanças heterogêneas e discretas no cérebro”, afirma Sheng. Segundo ele, o novo modelo foi projetado para “capturar essas variações com maior sensibilidade, adaptando-se dinamicamente às regiões mais afetadas pela doença” .
Um cérebro visto como rede
A inovação central do estudo está na forma como o cérebro é modelado. Em vez de analisar regiões isoladas, como fazem métodos tradicionais baseados em ressonância magnética estrutural (sMRI), o ANA-GNN interpreta o órgão como uma rede de interações entre diferentes áreas.
Essa abordagem permite identificar falhas de conectividade que precedem a degeneração visível. Regiões como o hipocampo, a amígdala e o córtex cingulado posterior — já conhecidas por sua relação com memória e cognição — foram destacadas pelo modelo como pontos críticos no desenvolvimento da doença .
“O diferencial está na capacidade de priorizar automaticamente regiões mais relevantes”, explica Haowen Zhong, coautor do estudo. “O sistema aprende quais áreas do cérebro têm maior peso no diagnóstico e ajusta sua análise de acordo com cada paciente.”
Base de dados robusta
Para validar o modelo, os pesquisadores utilizaram dados de 707 indivíduos provenientes do banco internacional ADNI (Alzheimer’s Disease Neuroimaging Initiative). A amostra incluiu 220 indivíduos cognitivamente normais, 378 com comprometimento cognitivo leve (MCI) e 109 diagnosticados com Alzheimer.
Os resultados mostram que o sistema não apenas distingue com precisão os diferentes estágios da doença, mas também mantém desempenho equilibrado entre os grupos. O F1-score, por exemplo, foi de 88,29% para indivíduos saudáveis, 83,17% para MCI e 87,57% para pacientes com Alzheimer .
Essa consistência é considerada um avanço importante, sobretudo no diagnóstico do MCI — estágio intermediário frequentemente difícil de identificar, mas crucial para intervenções precoces.
Integração de dados clínicos
Outro diferencial do ANA-GNN é a integração de dados não apenas de imagem, mas também clínicos e demográficos, como idade, sexo, nível educacional e testes cognitivos. Essa fusão multimodal é realizada por um mecanismo adaptativo que equilibra automaticamente o peso de cada tipo de informação.
“Em estágios iniciais, fatores clínicos podem ser mais relevantes do que alterações estruturais”, afirma Qiao Zhang, pesquisadora do Hospital de Pequim e coautora do trabalho. “Nosso modelo ajusta essa balança de forma dinâmica, o que aumenta a precisão do diagnóstico.”
Segundo o estudo, a remoção desses dados clínicos reduz drasticamente a acurácia do sistema para cerca de 68%, evidenciando o papel decisivo da abordagem integrada .
Superando limitações anteriores
Modelos anteriores de inteligência artificial aplicados ao Alzheimer, como redes convolucionais (CNNs), enfrentavam dificuldades para capturar relações complexas entre regiões cerebrais. Já as redes de grafos existentes utilizavam estruturas fixas, incapazes de refletir a heterogeneidade da doença.
O ANA-GNN supera essas limitações ao introduzir um mecanismo adaptativo que ajusta o “campo de visão” de cada região cerebral analisada. Isso permite que áreas mais afetadas agreguem mais informações, enquanto regiões menos relevantes têm sua influência reduzida.
Além disso, o modelo apresenta eficiência computacional: com apenas cerca de 35 mil parâmetros, ele supera sistemas mais complexos que chegam a ter mais de 140 mil parâmetros, mantendo tempo de inferência inferior a 0,3 milissegundos por amostra .
Imagem: Reprodução
Especialistas apontam que a principal contribuição do estudo está no potencial de aplicação clínica. Ferramentas como o ANA-GNN podem auxiliar médicos na detecção precoce da doença, permitindo intervenções antes que o dano cerebral seja irreversível.
A doença de Alzheimer, considerada uma das principais causas de demência no mundo, afeta milhões de pessoas e representa um desafio crescente para sistemas de saúde, especialmente com o envelhecimento da população global.
Apesar dos resultados promissores, os autores reconhecem limitações. O modelo foi testado em uma única base de dados e ainda precisa ser validado em populações diversas e em contextos clínicos reais. Além disso, a variabilidade entre equipamentos de imagem e protocolos médicos pode impactar o desempenho do sistema.
Entre as perspectivas futuras, os pesquisadores destacam a incorporação de novos tipos de dados, como exames PET e DTI, além da validação em estudos longitudinais para acompanhar a progressão da doença ao longo do tempo.
“Nosso objetivo é desenvolver uma ferramenta confiável, interpretável e acessível para uso clínico”, afirma Sheng. “A inteligência artificial não substitui o médico, mas pode ampliar significativamente sua capacidade de diagnóstico.”
Se confirmados em estudos adicionais, os resultados indicam que o futuro do diagnóstico do Alzheimer pode estar cada vez mais ligado à capacidade das máquinas de enxergar padrões invisíveis ao olhar humano — antecipando, com meses ou até anos de antecedência, os sinais de uma das doenças mais desafiadoras da atualidade.
Referência
Sheng, J., Zhong, H., Zhang, Q. et al. Rede neural gráfica de agregação de vizinhança adaptativa para diagnóstico precoce da doença de Alzheimer. Sci Rep (2026). https://doi.org/10.1038/s41598-026-50351-2